【SLAI Seminar】第二十八期回顾|染色质折叠的物理建模与AI预测:从三维森林模型到虚拟细胞计算
2026年3月10日上午,SLAI Seminar第二十八期在深圳河套学院成功举办。本次讲座由姬艳丽教授主持,特邀深圳湾实验室黄恺研究员,围绕“Chromatin folding: Physical modeling and AI prediction”主题,系统分享了其团队在四维基因组学、生物相分离机理以及应用人工智能解码生命体系等交叉领域的前沿研究成果与深刻洞见。

讲座简介
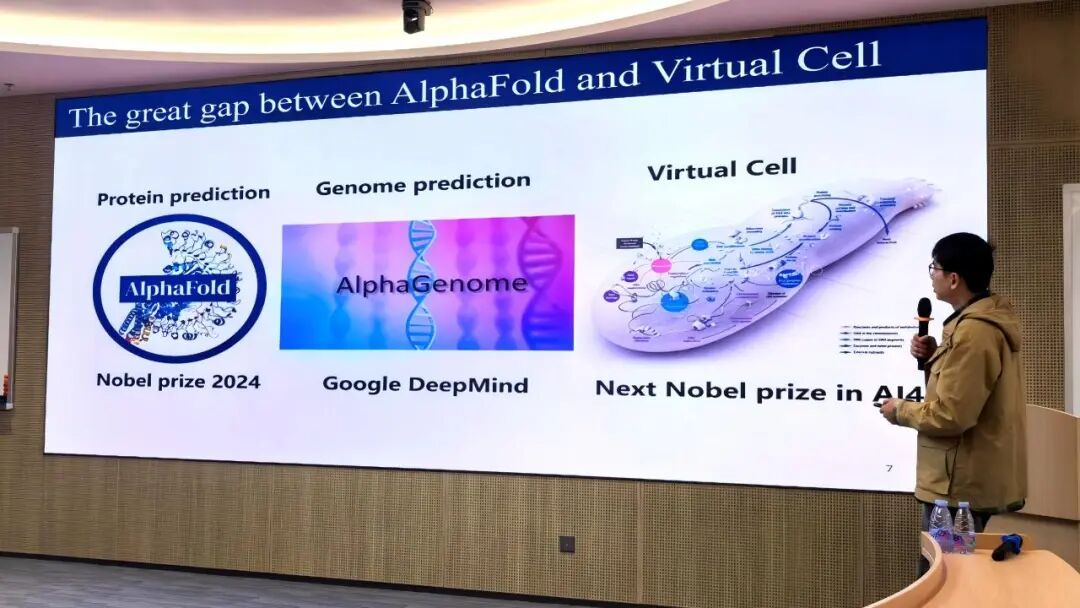
在人工智能重塑生命科学的浪潮下,构建能够全面模拟细胞行为的“虚拟细胞”正成为全球瞩目的前沿焦点。然而,相较于已经取得重大突破的蛋白质结构预测,基因组在三维空间中的动态折叠机制依然错综复杂,成为了通往“虚拟细胞”愿景的巨大科学鸿沟。
本次讲座中,黄恺研究员系统梳理了基因组多层次结构特征背后的物理学规律,重点介绍了其团队提出的“染色质三维森林模型”、基于图神经网络的多体互作预测方法以及对无序蛋白相变机制的深入探索。讲座生动展示了如何利用物理法则指导AI建模,进而为四维基因组学研究提供全新的理论框架与计算工具。
讲座内容
01 物理建模:破解染色质折叠的“三维森林”
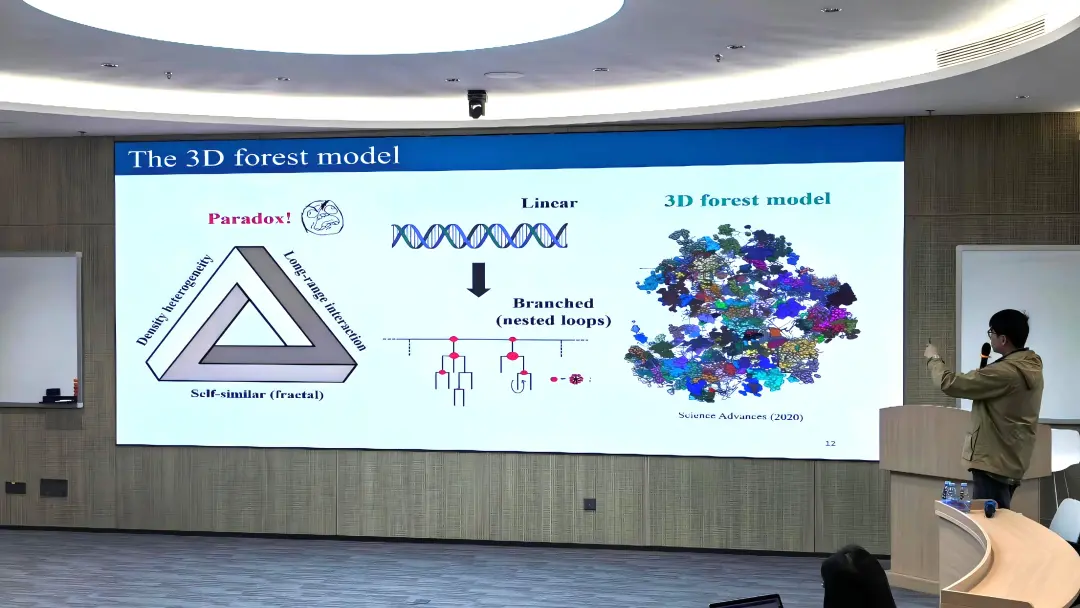
黄教授开篇指出,染色质作为遗传信息的物理载体,其动态三维结构直接调控着基因表达与DNA复制等关键生命过程。传统的高分子物理模型往往难以同时解释染色质在空间中表现出的长程互作、密度不均与自相似性等看似矛盾的高级结构特征。
为此,黄教授团队创新性地提出了染色质的三维森林模型。该模型认为基因组在受限的三维空间中形成了复杂的树状拓扑结构,进而从理论上完美统一了上述结构学特征。更重要的是,基于该物理模型,团队前瞻性地预测染色质在单细胞水平广泛存在多位点的高阶相互作用。这一违背传统二体互作认式的预测,随后被最新的多通道纳米孔测序实验所证实,确立了多体互作在基因调控中的普遍性。
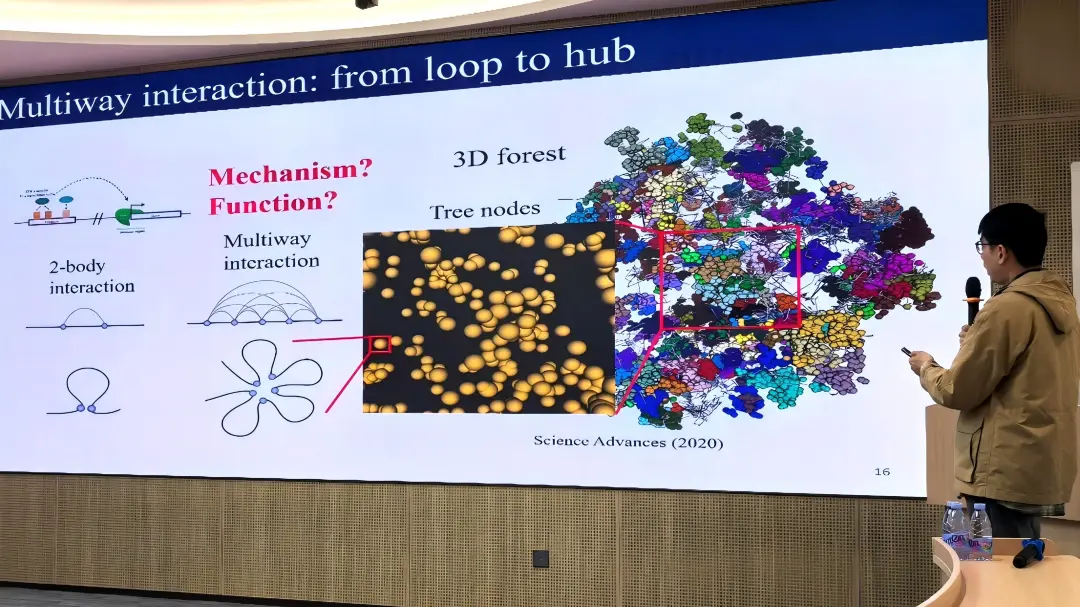
相分离机制:基因组多体互作的“催化剂”
在明确了多体互作的普遍性后,如何理解这些相隔极远的调控元件能在广袤的细胞核空间中精准相遇,成为了新的核心难题。黄教授团队跳出了传统的“转录工厂”静态假说,引入了生物相分离的动态视角。
研究表明,体内的反式调控因子或相关蛋白积累到一定浓度后,会在特定的调控元件区域发生液液相分离现象。这些形成的生物液滴通过融合效应将分散的顺式元件迅速拉拢到一起,触发转录后又迅速溶解。这种机制类似于化学反应中的酶催化过程,不仅极大地提高了远程调控元件协同激活基因表达的效率,也完美解释了活细胞成像中观测到的转录聚集体寿命短暂的实验现象。
AI驱动预测:图神经网络解码基因表达协同性
针对海量调控元件在多体互作中庞大的排列组合空间,单纯依靠实验穷举不仅成本高昂且难以实现。为此,黄教授团队巧妙整合了二维接触图谱与多维度的表观遗传数据,构建并训练了图神经网络模型,成功实现了对染色质多体互作的高效AI预测。
分析表明,许多极其遥远的增强子并非独立作用,而是通过高阶多体互作深度参与基因的协同表达调控。为了验证AI预测的准确性,团队采用CRISPRi技术对预测出的多个协同增强子进行了定点抑制实验。结果显示,单独抑制某一个增强子对基因表达影响有限,但当同时抑制特定的远程与近程增强子组合时,基因表达量出现了断崖式下降。这一现象高度契合了模型预测的非线性协同效应,为计算生物学的高效性提供了坚实的实验背书。
前沿探索:无序蛋白相变与生物启发的人工智能
讲座最后,黄教授还将视野拓展至大量参与相分离的无序蛋白。由于缺乏固定的三维结构,这些蛋白极易发生异常聚集,进而引发肿瘤与神经退行性疾病。团队开发了专门的AI模型来预测无序蛋白序列的相变能力,并成功定位了与致命突变密切相关的关键氨基酸位点,为未来的创新药物靶点发现开辟了新路径。
同时,黄教授提出了“基于生物学启发优化人工智能”的新颖构想。例如,相比于主流大语言模型在处理超长上下文时呈平方级爆炸的算力消耗,生命体在数十亿碱基对序列中寻找调控目标的注意力机制却展现出极高的时间效率。借鉴这种基因组级别的高效寻址规律来稀疏化并优化底层算法,有望为下一代AI模型架构提供灵感。
问答交流环节,与会师生围绕图神经网络的物理可解释性、无序蛋白序列特征提取机制以及数据驱动模式下的闭环挑战等议题,与黄研究员展开了热烈的讨论。
针对师生关于“AI模型复杂度与先验机制权衡”的提问,黄教授深刻指出,在当前高质量多组学数据相对匮乏的发展初期,盲目堆砌模型参数并非最优解。相反,将扎实的生物物理机制融入网络架构中,即便是小体量模型也能展现出惊人的预测泛化力。他同时呼吁,未来计算模型的迭代急需更丰富的多模态底层数据以及与高通量湿实验的紧密闭环验证。


本次讲座系统勾勒了从基础分子动力学到宏观四维基因组演化的全景图谱,展现了“物理假说指引方向、人工智能加速预测、前沿实验一锤定音”的现代交叉科学研究新范式。黄恺研究员团队的系列工作不仅深化了人类对生命暗物质的认知,更在数据科学与生命规律的碰撞中,向着构建精准可信的虚拟细胞迈出了坚实的一步。






